« Iodure de plomb(II) » : différence entre les versions
Pld (discuter | contributions) m + lien |
Fonctionnalité de suggestions de liens : 2 liens ajoutés. |
||
| Ligne 153 : | Ligne 153 : | ||
}}<!-- ----------------------------- Fin de l'infoboite ----------------------------- --> |
}}<!-- ----------------------------- Fin de l'infoboite ----------------------------- --> |
||
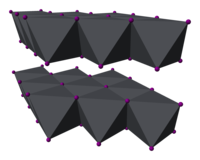
L''''iodure de plomb(II)''' est un composé inorganique de formule PbI<sub>2</sub>. C'est un solide jaune brillant à température ambiante qui devient rouge brique (de façon réversible) en le chauffant. Sous sa forme cristalline, il est utilisé dans les matériaux [[Détecteur à semi-conducteur|détecteurs]] de [[photon]]s à haute énergie comme les [[rayon X|rayons X]] et les [[rayon gamma|rayons gamma]]. |
L''''iodure de plomb(II)''' est un [[composé inorganique]] de formule PbI<sub>2</sub>. C'est un solide jaune brillant à température ambiante qui devient rouge brique (de façon réversible) en le chauffant. Sous sa forme cristalline, il est utilisé dans les matériaux [[Détecteur à semi-conducteur|détecteurs]] de [[photon]]s à haute énergie comme les [[rayon X|rayons X]] et les [[rayon gamma|rayons gamma]]. |
||
L'iodure de plomb est toxique dû au fait qu'il contient du [[plomb]]. Au {{s|XIX}}, il était utilisé par les artistes comme pigment sous le nom de « ''jaune d'iode'' », mais était trop instable pour être utile<ref name=Field> Salter, Thomas W., ''Field’s Chromatography: or Treatise on Colours and Pigments as Used by Artists By George Field. An entirely new and practical edition revised, rewritten and brought down to the present time'', 1869</ref>. |
L'iodure de plomb est toxique dû au fait qu'il contient du [[plomb]]. Au {{s|XIX}}, il était utilisé par les artistes comme [[pigment]] sous le nom de « ''jaune d'iode'' », mais était trop instable pour être utile<ref name=Field> Salter, Thomas W., ''Field’s Chromatography: or Treatise on Colours and Pigments as Used by Artists By George Field. An entirely new and practical edition revised, rewritten and brought down to the present time'', 1869</ref>. |
||
== Synthèse == |
== Synthèse == |
||
Version du 26 octobre 2022 à 01:13
| Iodure de plomb(II) | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| No CAS | ||
| No ECHA | 100.030.220 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | PbI2 | |
| Masse molaire[1] | 461 ± 0,1 g/mol I 55,06 %, Pb 44,95 %, |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
L'iodure de plomb(II) est un composé inorganique de formule PbI2. C'est un solide jaune brillant à température ambiante qui devient rouge brique (de façon réversible) en le chauffant. Sous sa forme cristalline, il est utilisé dans les matériaux détecteurs de photons à haute énergie comme les rayons X et les rayons gamma.
L'iodure de plomb est toxique dû au fait qu'il contient du plomb. Au XIXe siècle, il était utilisé par les artistes comme pigment sous le nom de « jaune d'iode », mais était trop instable pour être utile[2].
Synthèse

Il est possible de synthétiser l'iodure de plomb par réaction entre l'iodure de potassium (KI) et le nitrate de plomb(II) (Pb(NO3)2) :
2KI + Pb(NO3)2 → PbI2 + 2KNO3
En mélangeant des solutions de ces deux composés, on observe la formation d'un précipité d'iodure de plomb dans la solution.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Salter, Thomas W., Field’s Chromatography: or Treatise on Colours and Pigments as Used by Artists By George Field. An entirely new and practical edition revised, rewritten and brought down to the present time, 1869
